IIWポスターセッション受賞者寄稿 前川瑠里さん
2025年12月9日に開催された、東京大学知能社会国際卓越大学院プログラム (IIW) プログラム生を対象としたIIWポスターセッションにて、GCLS賞(優秀賞)を受賞された前川瑠里さんに研究紹介の記事を寄稿いただきました。
自己紹介
東京大学大学院工学系研究科先端学際工学専攻博士課程1年の前川瑠里と申します。学部3年時にジョージア工科大学に二度留学し、肺オルガノイドなどの3次元細胞モデルの研究に携わりました。その中で、従来の培養方法ではばらつきが大きく、創薬スクリーニングへの応用には課題があることを実感しました。こうした課題を解決したいと考え、修士課程からはマイクロ流体技術を活用して、小型で均質な3次元細胞モデルを大量に培養できるシステムの開発に取り組んでいます。さらに研究を進める中で、より大きな3次元細胞モデルについても、大規模かつ均一に作製できる技術の重要性に気づきました。その課題に取り組むために、春からはシアトルのワシントン大学で、より大きな3次元培養モデルである胚モデルを対象としたシステム開発の研究に取り組みます。
プレゼンの概要
背景
3次元細胞モデルは、生体内の生理機能や細胞間相互作用をより忠実に再現できるため、薬物スクリーニングや疾患解析に不可欠です。がんなどの模倣モデルであるスフェロイドに加え、臓器特異的な構造を持つオルガノイド、初期発生を模倣するガストルロイド(胚様体モデル)など、高度な生体模倣システムの開発が進んでいます。創薬におけるハイスループットスクリーニング(HTS)を実現するには、これらの3次元細胞モデルを大量かつ均一に生成する技術が求められます。しかし、従来のウェル法やハンギングドロップ法では、数万規模での安定供給は困難でした。
技術的障壁
この解決策として、中空ハイドロゲルカプセル法を用いたマイクロ流体技術が期待されています。しかし従来法では、特殊なキャピラリー加工や多層PDMSデバイスの製作、精密な流速制御、さらに煩雑なパラメータ調整が必要です。そのため、工学を専門としない一般的な生物学ラボが日常的なツールとして導入・運用するには、設備面・技術面の両方で極めて高い障壁がありました。
本研究
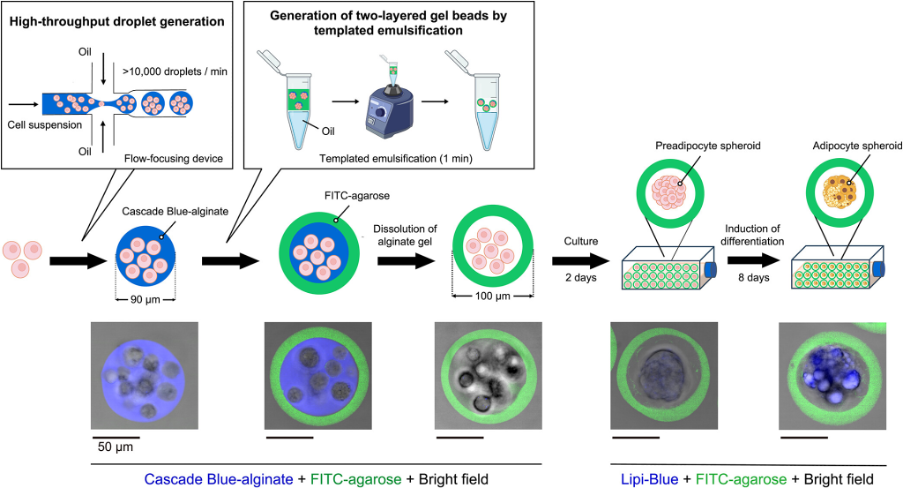
本研究では、簡便なマイクロ流体デバイスとボルテックスを利用したテンプレート乳化法を組み合わせることで、均一な3次元細胞モデルを大規模に作製する新しいプラットフォームを開発しました(図1)。本手法ではまず、マイクロ流体デバイスによる液滴生成技術を用いて、細胞をアルギン酸コア内に封入します。このときの生成速度は毎分1万個以上です。次に、これを核としてアガロース液中に再封入し、ボルテックス乳化によってアルギン酸とアガロースの二層構造を迅速に形成させます。アガロースをゲル化した後、内部のアルギン酸を溶解することで、「中空アガロースカプセル」が得られます。カプセル内の細胞は24時間以内に重力によって自発的に凝集し、均一な3次元細胞モデルを形成します。
本システムで作成したスフェロイドを大規模画像解析パイプラインによって評価した結果、直径60 µmのスフェロイドを10万個以上生成することに成功しました。形成成功率は90%を超え、サイズ均一性も極めて高く(CV < 11%)、高品質なスフェロイドを安定して作製できることが示されました。さらに、分化8日後のサイズの均一性は従来法と比較してCV値で20%改善しました。分化したスフェロイドの脂質蓄積(Lipi-Blue蛍光強度)は従来法よりも有意に高く(p = 0.0198)、本システムが分化を促進することも確認されました。また、iPS細胞由来スフェロイドや腸管オルガノイドの培養にも成功しており、600 µm以上のアルギン酸コアを用いることで、ガストルロイドなどの比較的大きな胚発生を模倣したモデルの生成にも適用できる可能性が示されました。このカプセル内での胚モデルの生成に関してはより詳細な検証を今後進める予定です。
結論として、本システムは、スフェロイドからオルガノイド、さらにはガストルロイドに至るまで、さまざまな3次元細胞モデルを作製・分化させるためのスケーラブルなアプローチを提供します。iPS細胞由来のスフェロイドやオルガノイドを大規模に生成できることで、がんや代謝疾患などに対する高精度な疾患モデリングが可能になります。また、ガストルロイドのような初期発生モデルのスクリーニングは、発生異常に関する新たな知見をもたらすと考えています。
このカプセル培養システムが、ハイスループットスクリーニング、創薬、そしてバイオプリンティングを基盤とした組織工学における新たな展開を生み、次世代の培養技術を牽引する基盤へと発展していくことを願っています。私自身も、その一端を担えるよう尽力していきたいと考えています。
プレゼンの工夫
この研究分野で何がすでに実現されており、どのような課題を自分の研究では解決しようとしているのかが明確に伝わるよう意識して構成しました。加えて、専門の異なる方々にも理解していただけるよう、まずは広い一般的な背景から導入し、徐々に研究の核心へと焦点を絞り込み、最後に再びより大きな文脈へと接続することで、本研究の意義と将来性が自然に伝わるよう工夫しました。
副賞の活用方法
副賞につきましては、春からシアトルで研究を行う際の旅費として、大切に使わせていただきます。このような形で私の研究活動を支援していただけることに、改めて心より感謝申し上げます。今後も何らかの形で協働させていただけましたら大変嬉しく存じます。ありがとうございました。
寄稿:前川瑠里